Thiết kế Phòng sạch sản xuất Vắc xin như thế nào
Sản xuất vắc xin cần một môi trường kiểm soát đủ tốt. Do vậy việc xây dựng, thiết kế phòng sạch sản xuất vắc xin là điều cần thiết đối với các cơ sở này.
Các bệnh truyền nhiễm với tốc độ lây lan nhanh luôn là một mối nguy hiểm luôn phải đề phòng, chúng ta có thể thấy nó qua dịch Covid 19. Đó là lý do các nhà phát triển vắc xin hàng ngày đang ngày càng phải phá vỡ các giới hạn để cung cấp nhiều phương pháp điều trị giúp kích thích và bảo vệ hệ thống miễn dịch của con người một cách an toàn, hiệu quả và nhất quán.
Tuy nhiên, chúng ta ở đây sẽ không nói quá nhiều đến vắc xin và tác dụng của chúng mà là làm sao để tạo ra được một môi trường để sản xuất ra vaccine. Do đó hãy cùng chúng tôi tìm hiểu các chú ý khi thiết kế phòng sạch vắc xin và cơ sở sản xuất vắc xin nhé.
Vắc xin và các giai đoạn phát triển của nó
Vắc xin là gì?
Vắc xin là một chế phẩm sinh học cung cấp khả năng miễn dịch thu được chủ động đối với một bệnh truyền nhiễm cụ thể. Vắc xin thường chứa tác nhân giống vi sinh vật gây bệnh và thường được tạo ra từ các dạng vi sinh vật, độc tố hoặc một trong các protein bề mặt của nó, mà đã bị làm suy yếu hoặc bị giết chết.
Tác nhân này kích thích hệ thống miễn dịch của cơ thể, sau khi coi tác nhân là một mối đe dọa, sẽ tiêu diệt nó và sẽ tiếp tục nhận ra và tiêu diệt bất kỳ vi sinh vật nào có liên quan đến tác nhân đó mà nó có thể gặp trong tương lai. Vắc xin có thể mang tính dự phòng (để ngăn ngừa hoặc cải thiện ảnh hưởng của một chứng lây nhiễm trong tương lai bởi một mầm bệnh "hoang dã" trong tự nhiên), hoặc mang tính điều trị (để chống lại một căn bệnh đã xảy ra, chẳng hạn như ung thư).
Các giai đoạn phát triển của vắc xin
Giai đoạn phát triển đầu tiên là giai đoạn khám phá bao gồm nghiên cứu ban đầu, nơi các nhà khoa học hoặc nhà nghiên cứu xác định một kháng nguyên có thể giúp ngăn ngừa hoặc điều trị bệnh. Sau khi xác định được kháng nguyên, bước tiếp theo là giai đoạn tiền lâm sàng.
Trong giai đoạn tiền lâm sàng, các nhà khoa học sử dụng hệ thống nuôi cấy mô hoặc tế bào cùng với thử nghiệm trên động vật để đánh giá mức độ an toàn của vắc xin tiềm năng. Sau khi hoàn thành, một nhà phát triển vắc xin sẽ yêu cầu một Đơn đăng ký Thuốc Mới Điều tra từ FDA (Mỹ) và các tổ chức liên quan khác. Từ đây, vắc-xin tiềm năng bắt đầu bước vào giai đoạn phát triển lâm sàng.
Giai đoạn phát triển lâm sàng bao gồm ba giai đoạn liên quan đến việc đánh giá vắc xin ứng cử viên ở người với mục tiêu an toàn và xác định loại và mức độ đáp ứng miễn dịch. Một số xét nghiệm trong các giai đoạn này bao gồm liều lượng, lịch trình, phương pháp phân phối và khả năng sinh miễn dịch. Các nhóm thử nghiệm sẽ bắt đầu với quy mô nhỏ và sẽ xây dựng trong các giai đoạn tiếp theo.
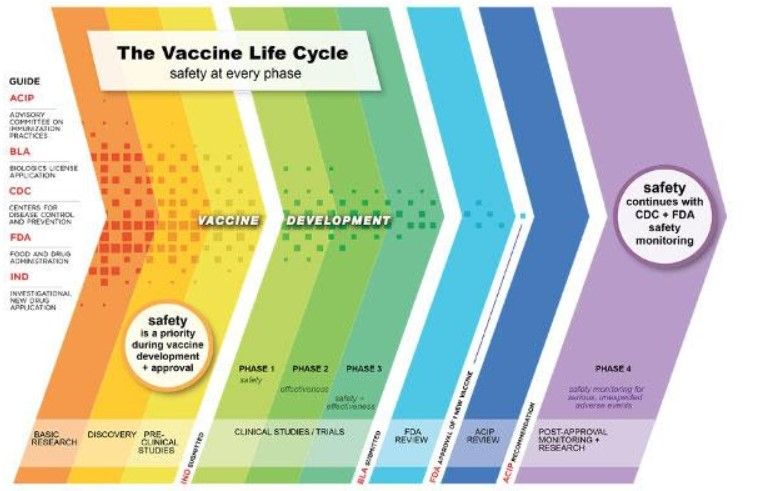
Sau khi Giai đoạn 3 thành công, nhà phát triển vắc xin sẽ nộp Đơn đăng ký Giấy phép Sinh học cho FDA và các tổ chức liên quan khác, nơi vắc xin sẽ được xem xét và thử nghiệm để xem liệu vắc xin có đáp ứng các thông số kỹ thuật của họ hay không. Một số thử nghiệm này có thể kể đến như:
- Kiểm tra danh tính
- Kiểm tra độ tinh khiết
- Kiểm tra vi sinh vật
- Kiểm tra độ vô trùng
Sau khi được phê duyệt, vắc xin sẽ chuyển sang sản xuất và hệ thống kiểm soát chất lượng sẽ được thiết lập.
Một số cân nhắc trước khi thiết kế cơ sở sản xuất vắc xin
Giống như bất kỳ môi trường sản xuất dược phẩm hoặc công nghệ sinh học nào khác, sản xuất vắc xin cũng yêu cầu các khu vực phòng sạch dành riêng. Và việc sản xuất các loại thuốc sinh học sẽ mang đến những thách thức lớn cho thiết kế phòng sạch.
Lưu ý khi thiết kế cơ sở sản xuất vắc xin
Tất cả các giai đoạn nghiên cứu và sản xuất vắc xin đều cần có phòng sạch để mang lại môi trường làm việc tốt nhất. Nhiệt độ, độ ẩm, luồng không khí, áp suất không khí (dương hoặc âm tùy thuộc vào mức BSL), và các yêu cầu môi trường khác là những yêu cầu bắt buộc phải đáp ứng để cung cấp vắc xin an toàn mà không có bất kỳ nguy cơ ô nhiễm nào.
Và dưới đây là một số điều cần lưu ý khi bố trí cơ sở sản xuất vắc xin hoặc cơ sở sản xuất sinh phẩm:
- Loại vắc xin hoặc thành phần sản xuất
- Mức độ an toàn sinh học (BSL) tùy thuộc vào loại vắc xin hoặc vectơ vi rút được sử dụng
- Các mẫu quy trình làm việc
- Phân loại ISO / yêu cầu GMP đối với phòng sạch vắc xin
- Giai đoạn quy trình (R & D, giai đoạn tiền lâm sàng và lâm sàng, sản xuất quy mô lớn)
- Kích thước, thiết bị bên trong phòng, số người làm việc bên trong
- Năng lực sản xuất vắc xin / số liều dự kiến sản xuất
- Mở rộng cơ sở
- Các tiện ích tiêu chuẩn (hệ thống ống nước, điện, khí xử lý, v.v.)

Cân nhắc thiết kế phòng sạch vắc xin điển hình
Phòng sạch vắc xin là môi trường được xây dựng có mục đích được tùy chỉnh theo một quy trình nghiêm ngặt. Mặc dù mỗi phòng sạch vắc xin đều sẽ có những cách tiếp cận khác nhau, tuy nhiên vẫn có những cân nhắc chung trong phòng sạch đối với các ứng dụng và nền tảng công nghệ.
Các cân nhắc khi thiết kế phòng sạch vắc xin
- MAL (Material Airlocks) / PAL (Personnel Airlocks)
- Các mô hình cửa interlock và luồng nhân sự
- Áp suất phòng sạch
- Quy trình cấu hình và lắp đặt thiết bị
- Cấu hình HVAC và phân tách luồng không khí
- Dispensing Booth hoặc LAF
- Thiết kế luồng khí hồi
- Quá trình phân phối
- Kiểm soát môi trường
- Phân loại ISO, nhiệt độ và độ ẩm
- Xem, giám sát, camera an ninh
- Giao thức cấp và làm sạch
Một số chú ý, kinh nghiệm cho hệ thống cơ sở vắc xin.
- N + 1 tiện ích dự phòng
- Lò phản ứng sinh học
- Xử lý bảng tiện ích & móc phân phối
- Tạo và phân phối WFI (Water for Injection)
- VHP (Hơi Hydrogen Peroxide)
- BMS (Hệ thống quản lý tòa nhà) và khóa cửa liên động
- Thiết bị giám sát môi trường (máy đếm hạt tồn tại và không thể sống được)
- Thiết bị phân tích
- Thiết kế và bố trí cơ sở sản xuất vắc xin
Xem thêm: Phòng sạch dược phẩm vô trùng
Thiết kế và bố trí cơ sở sản xuất Vắc xin
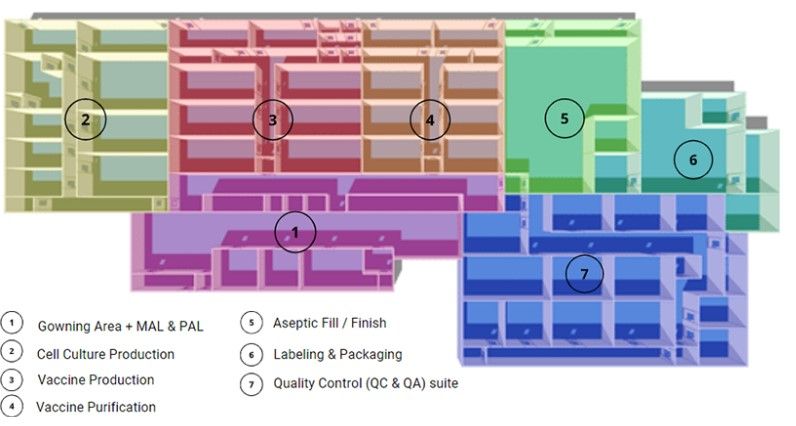
Phòng thay đồ trong phòng sạch / Khu vực ủ:
Giống như bất kỳ môi trường phòng sạch nào khác, cơ sở sản xuất vắc xin sẽ cần khu vực ủ để loại bỏ nguy cơ ô nhiễm. Cần phải sử dụng nhiều Air Lock trong thiết kế, Air lock cho vật liệu (MAL) và Air Lock cho nhân sự (PAL).
Sản xuất nuôi cấy tế bào:
Đây là nơi loại bỏ các tế bào, mô hoặc cơ quan từ động vật hoặc thực vật và đặt chúng vào môi trường nhân tạo để thúc đẩy tăng trưởng. Phòng sạch nuôi cấy tế bào lý tưởng là một khu vực tách biệt, như bạn có thể thấy trong hình bố trí ở trên. Kích thước phòng sạch sẽ bị ảnh hưởng bởi số lượng, kích thước của lò phản ứng sinh học hoặc thiết bị lên men nuôi cấy tế bào. Công suất xử lý sinh học thông thường từ 50 đến 2.000 lít và thậm chí hơn thế nữa.
Sản xuất vắc xin:
Đây là khu vực phòng sạch của cơ sở sản xuất vắc xin, vi rút được sử dụng để thu hoạch và bất hoạt các mầm bệnh bên trong nó. Giả sử, bạn đang sản xuất vắc xin với các vectơ vi rút, tùy thuộc vào chủng vi rút; bạn sẽ cần phải suy nghĩ về cấp độ an toàn sinh học (BSL) và các yêu cầu về GMP hiện tại trong thiết kế và bố trí nhà máy vắc xin. Mức BSL sẽ ảnh hưởng đến hệ thống HVAC và thiết kế cơ sở vắc xin, vì phòng sạch có thể cần áp suất âm cho BSL-3 và BSL-4. Phân loại cấp độ sạch phòng sạch cho các hoạt động tiêm chủng này thường là Cấp C (ISO7).

Tinh chế vắc xin:
Tinh chế vắc xin là một trong những nhiệm vụ khó khăn nhất vì nó thường đòi hỏi nhiều bước thanh lọc và làm sạch. Tuy nhiên các tiến bộ công nghệ hiện nay có thể đẩy nhanh quá trình này. Và các cơ sở sản xuất vắc xin sẽ cần thiết bị sắc ký khí cho bước này.
Công thức vắc xin, trong đó chất bổ trợ, chất ổn định, chất bảo quản được thêm vào vắc xin, sẽ diễn ra trong phòng sạch này. Giám sát môi trường cũng là điều cần xem xét trong quá trình thiết kế / bố trí.
Đổ đầy / hoàn thiện vô trùng:
Trong cơ sở sản xuất vắc xin cần bao gồm một khu vực cụ thể để đổ và hoàn thiện vô trùng cho quá trình tiệt trùng và đóng gói vắc xin mới được sản xuất. Phòng sạch vô trùng là khu vực quan trọng của cơ sở để đảm bảo sự an toàn của vắc xin bên trong các lọ và ống tiêm.
Trong khu vực này, HVAC sẽ được thiết kế và vận hành để bảo vệ cho lõi vô trùng bằng cách sử dụng áp suất dương. Cần phải có tủ an toàn sinh học hoặc Laminar Air Flow System để có tạo ra khu vực ISO 5 (Cấp A) cho các hoạt động quan trọng của quá trình chiết rót, với nền phòng sạch ISO 8 (Cấp D).
Ghi nhãn và đóng gói:
Mặc dù khu vực này không cần phải tuân theo một cấp độ sạch cụ thể nào, tuy nhiên nó cũng là một phần quan trọng của thiết kế cơ sở sản xuất vắc xin. Trước tiên chúng ta cần đảm bảo rằng vắc xin phù hợp sẽ được đựng trong đúng lọ có nhãn phù hợp. Cấp phòng sạch không được phân loại (CNC - Clean Non-Classified) hoặc chưa được phân loại (UNC - Unclassified) cần tuân theo các hướng dẫn của WHO , tùy thuộc vào việc đóng nắp vắc xin có được thực hiện hay không.
Thông thường, việc đóng nắp sẽ được thực hiện trong giai đoạn trước của quá trình sản xuất vắc xin. Nhà máy sản xuất vắc xin sẽ cần máy đóng gói, dán nhãn lọ và thiết bị bảo quản lạnh như tủ đông (vắc xin mới hơn cần được giữ ở -70 ° C / - 94 ° F).
Bộ kiểm soát chất lượng (QC & QA):
Bộ kiểm soát chất lượng rất cần thiết để kiểm tra hiệu lực của vắc xin đang được sản xuất. Cơ thể sống và thuốc sinh học phức tạp hơn nhiều so với thuốc hóa học. Phản ứng của các sinh vật sống bên trong các lọ có thể khác nhau trong mỗi đợt sản xuất vắc xin, và đó là lý do tại sao chúng cần được kiểm tra cẩn thận. Trong một khu vực mở, phòng thí nghiệm kiểm soát chất lượng cần có phòng sạch cấp A trên nền cấp B. Trong phòng thí nghiệm QC riêng biệt và chuyên dụng, sẽ sử dụng khu vực cách ly trên nền cấp D.
Xem thêm:




















